
-

╔·╬’═©╣┘╬ó
┼Ń─ŃūźūĪ╔·├³┐Ų╝╝
╠°äėĄ─├}▓½
Arraystar rG4ąŠŲ¼Ż║ĮŌµiRNAäėæBĮYśŗŖW├ž
ĪŠūų¾wŻ║ ┤¾ ųą ąĪ Ī┐ ĢrķgŻ║2025─Ļ12į┬16╚š üĒį┤Ż║┐Ą│╔╔·╬’
ŠÄ▌ŗ═Ų╦]Ż║
ĪĪĪĪArraystar rG4ąŠŲ¼╝╝ąg▓╗āH─▄ē“ėąą¦▓Č½@║═Öz£y╗Ņ╝Ü░¹ųąĄ─rG4Ż¼═¼Ģrę▓Ž¹│²┴╦DMSšTī¦Ą─ą▐’Ś╦∙«a╔·Ą─Ų½▓ŅŻ¼Å─Č°’@ų°╠ßĖ▀┴╦rG4 Č©┴┐łDūVĘų╬÷ĮY╣¹Ą─£╩┤_ąį║═┐╔┐┐ąįĪŻ
ę╗Īó║åĮķ
RNA G-╦─┬ō¾w (RNA G-quadruplexesŻ¼rG4)╩Ūė╔Ė╗║¼°BÓč▀╩ (G) Ą─RNAą“┴ą═©▀^HoogsteenÜõµIą╬│╔Ą─ę╗ĘNĘŪĮøĄõČ■╝ēĮYśŗĪŻįōĮYśŗė╔Čč»BĄ─G-╦─Ęų¾wŲĮ├µśŗ│╔Ż¼▓óė╔K⁺Ą╚å╬ārĻ¢ļxūėĘĆČ©Ż©łD1Ż®ĪŻrG4Ą─äėæBĮYśŗ▐Dūā┐╔š{┐žRNA▐Dõø[1]Īó╚Š╔½┘|ą▐’Śę“ūė─╝╝»[2]ĪómiRNAŪ░¾w╝ė╣ż[3]ĪómRNAĘŁūg[4, 5]ęį╝░ mRNA ĘĆČ©ąį[6]ĪŻ┤╦═ŌŻ¼rG4 ▀Ć─▄┼cm7G [3]Īóo8G[7]║═m6A[8, 9]Ą╚ RNA ą▐’Ś╣▓═¼š{┐ž╗∙ę“▒Ē▀_ĪŻrG4ą╬│╔░l╔·╩¦š{Ż¼ätĢ■ė░Ēææ¬╝żĘ┤æ¬ [7]Īó░®░Y╗∙ę“▒Ē▀_š{┐ž [10, 11]Ż¼▓ó┼c┼┴Į╔Ł▓ĪĪó┬Ęęū¾w░V┤¶╝░ČÓŽĄĮy╬«┐sųą░l╔·Ą─”┴-═╗ė|║╦Ą░░ūŠ█╝»ėąĻP[12]ĪŻ
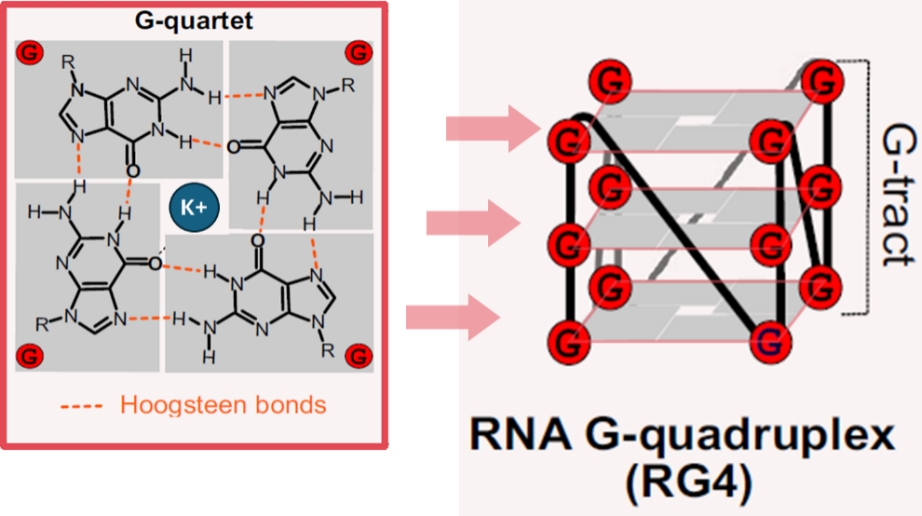
łD1. į┌Ė╗║¼°BÓč▀╩Ą─RNAą“┴ąųąŻ¼╦─éĆ°BÓč▀╩═©▀^HoogsteenµIĮY║Žą╬│╔G-╦─Ęų¾wŲĮ├µŻ¼G-╦─Ęų¾wŲĮ├µČč»Bą╬│╔RNA G-╦─┬ō¾wŻ©RG4Ż®[13]ĪŻ
Arraystar rG4ąŠŲ¼╝╝ąg┐╔Š½£╩Č©┴┐▐DõøĮMųąĄ─rG4 ĮYśŗĪŻŲõųąĄ─ĻPµI▓Į¾E░³└©Ż║¾wā╚┴“╦ßČ■╝ū§ź (Dimethyl sulfate, DMS) ╠Ä└ĒĪó¾w═ŌRNAųžš█»BŻ¼ęį╝░╩╣ė├┐╣G4┐╣¾wŻ©BG4Ż®▀MąąėH║═ąį▓Č½@ĪŻļS║¾Ż¼īó▓Č½@ĄĮĄ─║¼ėą rG4ĮYśŗĄ─ RNA▀Mąą╚ź╝ū╗∙╗»╠Ä└ĒŻ¼ęį╚ź│² DMS ╠Ä└Ē╦∙«a╔·Ą─Ė▒«a╬’m1A/m3CŻ¼Ž¹│²Ųõįņ│╔Ą─Öz£yĖ╔ö_ĪŻūŅ║¾Ż¼└¹ė├Ė▀ņ`├¶Č╚Ą─Arraystar rG4 ąŠŲ¼╠Įßśī”rG4-RNA▀MąąČ©┴┐Ęų╬÷ĪŻArraystar rG4ąŠŲ¼╝╝ąg▓╗āH─▄ē“ėąą¦▓Č½@║═Öz£y╗Ņ╝Ü░¹ųąĄ─rG4Ż¼═¼Ģrę▓Ž¹│²┴╦DMSšTī¦Ą─ą▐’Ś╦∙«a╔·Ą─Ų½▓ŅŻ¼Å─Č°’@ų°╠ßĖ▀┴╦rG4 Č©┴┐łDūVĘų╬÷ĮY╣¹Ą─£╩┤_ąį║═┐╔┐┐ąįĪŻ

Č■Īó╝╝ągā×ä▌
¾wā╚DMS╠Ä└Ē┼c¾w═Ōųžš█»BÅ═¼F┴╦šµīŹĄ─rG4ĮYśŗ
╩╣ė├Ė▀ėH║═ąįĄ─BG4┐╣¾w╠ž«ÉąįĖ╗╝»║¼ėąrG4ĮYśŗĄ─RNA
Demthylation╠Ä└Ē╚ź│²┴╦DMS ╠Ä└ĒĄ─Ė▒«a╬’m1A/m3C╦∙įņ│╔Ą─Öz£yĖ╔ö_
Arraystar ąŠŲ¼┐╔ęįņ`├¶Ą─Öz£yrG4 RNA, ░³└©RNA£yą“¤oĘ©£╩┤_Öz£yĄ─Ą═žSČ╚RNA
╚²ĪóīŹ“×┴„│╠
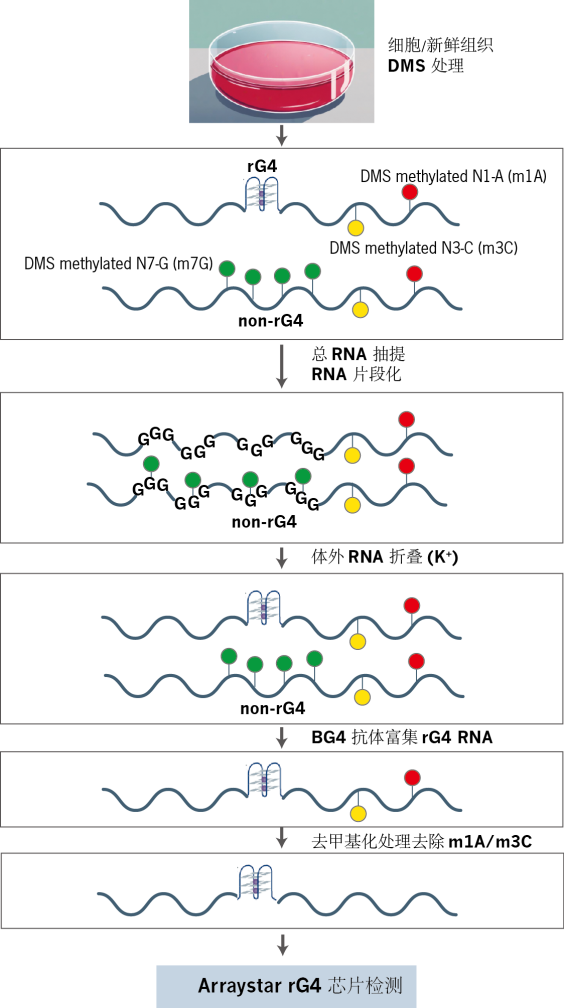
łD2. rG4ąŠŲ¼īŹ“×┴„│╠łDĪŻ
1. ¾wā╚ DMS ╠Ä└Ē
┼ÓB╝Ü░¹Įø┴“╦ßČ■╝ū§źŻ©DMSŻ®╠Ä└ĒŻ¼ī” RNA ųąĄ─Ž┘Óč▀╩Ż©AŻ®Īó░¹ÓūÓżŻ©CŻ®╝░ĘŪ rG4š█»Bģ^ė“Ą─°BÓč▀╩Ż©GŻ®▀Mąą╝ū╗∙╗»ą▐’ŚĪŻrG4 ĮYśŗā╚Ą─ G ēA╗∙ę“┐šķg╬╗ūĶ▓╗╩▄ė░ĒæŻ¼Å─Č°▒Ż┴¶Ųõ╬┤╝ū╗∙╗»ĀŅæBĪŻ
2. RNA │ķ╠ß┼c¾w═Ōųžš█»B
Ęųļx┐é RNA ▓ó▀MąąŲ¼Č╬╗»╠Ä└ĒŻ¼ļS║¾į┌║¼K⁺Ą─ŠÅø_¾wŽĄųąĮøÜvūāąį-Å═ąį▀^│╠ĪŻ┤╦▓Į¾EāHį╩įS╝Ü░¹ā╚įŁėąĄ─ rG4 ģ^ė“╠ž«Éąįųžš█»BŻ¼Č°Ųõ╦¹ģ^ė“ė╔ė┌öyĦm7Gą▐’ŚŻ¼¤oĘ©ą╬│╔ĘĆČ©ĮYśŗĪŻ
3. rG4 ├Ōę▀│┴ĄĒ
└¹ė├┐╣ G-╦─┬ō¾w┐╣¾wŻ©BG4Ż®ī”║¼ rG4 ĮYśŗĄ─ RNA ▀Mąą├Ōę▀│┴ĄĒŻ©IPŻ®Ż¼īŹ¼F─┐ś╦ĘųūėĄ─╠ž«ÉąįĖ╗╝»ĪŻ
4. ╚ź╝ū╗∙╗»┼cĘ┤▐Dõø
Ė╗╝»Ą─ RNA Įø╚ź╝ū╗∙╗»├Ė╠Ä└ĒŻ¼ŪÕ│² DMS šTī¦Ą─Ė▒«a╬’Ż©╚ń m¹A/m³CŻ®Ż¼Ž¹│²Öz£yŲ½▓ŅĪŻļS║¾═©▀^Ę┤▐Dõø║Ž│╔ļpµ£ cDNAŻ¼▓óę²╚ļT7 åóäėūėą“┴ąĪŻ
5. ¤╔╣Ōś╦ėø cRNA ║Ž│╔
ęį cDNA ×ķ─Ż░ÕŻ¼T7 RNA Š█║Ž├Ė┤▀╗»¾w═Ō▐DõøĘ┤æ¬Ż¼ōĮ╚ļCy3-CTP ¤╔╣Ō╚Š┴ŽŻ¼╔·│╔ĦCy3 ś╦ėøĄ─Ę┤┴x cRNAĪŻ
6. ąŠŲ¼ļsĮ╗┼cöĄō■Ęų╬÷
ś╦ėøĄ─ cRNA ┼cArraystar rG4 ąŠŲ¼ļsĮ╗Ż¼═©▀^¤╔╣Ōą┼╠¢Č©┴┐Ęų╬÷▐DõøĮMųąrG4 ĮYśŗĄ─Ęų▓╝┼cžSČ╚ĪŻ
╦─ĪóąŠŲ¼ģóöĄ
Arraystar ╚╦ŅÉ rG4 ąŠŲ¼ģóöĄ
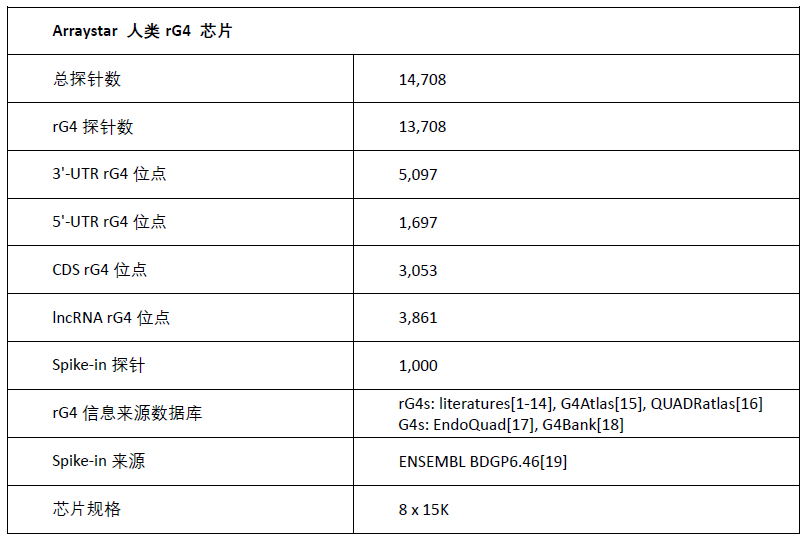
RNA G-quadruplex (rG4) öĄō■Äņ
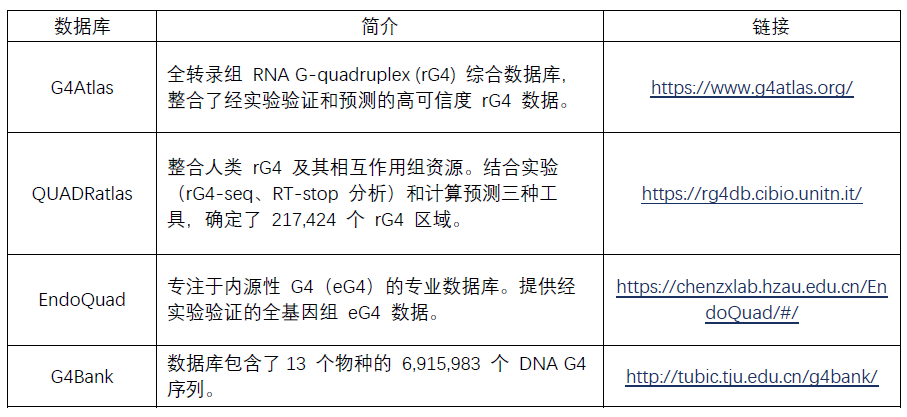
ģó┐╝╬─½I
1. Yari H et al: LncRNA REG1CP promotes tumorigenesis through an enhancer complex to recruit FANCJ helicase for REG3A transcription. Nat Commun 2019, 10(1):5334.[PMID: 31767869]
2. Lee YW, Weissbein U, Blum R, Lee JT: G-quadruplex folding in Xist RNA antagonizes PRC2 activity for stepwise regulation of X chromosome inactivation. Mol Cell 2024, 84(10):1870-1885 e1879.[PMID: 38759625]
3. Pandolfini L et al: METTL1 Promotes let-7 MicroRNA Processing via m7G Methylation. Mol Cell 2019, 74(6):1278-1290 e1279.[PMID: 31031083]
4. Arora A, Suess B: An RNA G-quadruplex in the 3' UTR of the proto-oncogene PIM1 represses translation. RNA Biol 2011, 8(5):802-805.[PMID: 21734463]
5. Song J, Perreault JP, Topisirovic I, Richard S: RNA G-quadruplexes and their potential regulatory roles in translation. Translation (Austin) 2016, 4(2):e1244031.[PMID: 28090421]
6. Rouleau S et al: 3' UTR G-quadruplexes regulate miRNA binding. RNA 2017, 23(8):1172-1179.[PMID: 28473452]
7. Ma Y et al: RNA G-Quadruplex within the 5'-UTR of FEN1 Regulates mRNA Stability under Oxidative Stress. Antioxidants (Basel) 2023, 12(2).[PMID: 36829835]
8. Yoshida A et al: Recognition of G-quadruplex RNA by a crucial RNA methyltransferase component, METTL14. Nucleic Acids Res 2022, 50(1):449-457.[PMID: 34908152]
9. Jara-Espejo M, Fleming AM, Burrows CJ: Potential G-Quadruplex Forming Sequences and N(6)-Methyladenosine Colocalize at Human Pre-mRNA Intron Splice Sites. ACS Chem Biol 2020, 15(6):1292-1300.[PMID: 32396327]
10. Anastasakis DG et al: Nuclear PKM2 binds pre-mRNA at folded G-quadruplexes and reveals their gene regulatory role. Mol Cell 2024, 84(19):3775-3789 e3776.[PMID: 39153475]
11. Kharel P, Ivanov P: PKM2-G-quadruplex interactions conspire to regulate the cancer transcriptome. Mol Cell 2024, 84(19):3574-3575.[PMID: 39366344]
12. Matsuo K et al: RNA G-quadruplexes form scaffolds that promote neuropathological alpha-synuclein aggregation. Cell 2024, 187(24):6835-6848 e6820.[PMID: 39426376]
13. Dumas L et al: G-Quadruplexes in RNA Biology: Recent Advances and Future Directions. Trends Biochem Sci 2021, 46(4):270-283.[PMID: 33303320]
14. Kwok CK et al. rG4-seq reveals widespread formation of G-quadruplex structures in the human transcriptome. Nat. Methods 13, 841©C844 (2016).
15. Yang SY et al. Transcriptome-wide identification of transient RNA G-quadruplexes in human cells. Nat. Chem. Biol. 14, 180©C183 (2018).
16. Yeung PY et al. Systematic evaluation and optimization of the experimental steps in RNA G-quadruplex structure sequencing. Sci. Rep. 9, 8091 (2019).
17. Weng X et al. Keth-seq for transcriptome-wide RNA structure mapping. Nat. Chem. Biol. 16, 489©C492 (2020).
18. Hansel-Hertsch R et al. G-quadruplex structures mark human regulatory chromatin. Nat. Genet. 48, 1267©C1272 (2016).
19. Herviou P et al. hnRNP H/F drive RNA G-quadruplex-mediated translation linked to genomic instability and therapy resistance in glioblastoma. Nat. Commun. 11, 2661 (2020).
20. Simko EAJ et al. G-quadruplexes offer a conserved structural motif for NONO recruitment to NEAT1 architectural lncRNA. Nucleic Acids Res. 48, 7421©C7438 (2020).
21. Bolduc F et al. The small nuclear ribonucleoprotein polypeptide A (SNRPA) binds to the G-quadruplex of the BAG-1 5'UTR. Biochimie 176, 122©C127 (2020).
22. Guo JU et al. RNA G-quadruplexes are globally unfolded in eukaryotic cells and depleted in bacteria. Science. Sep 23;353(6306):aaf5371 (2016).
23. von Hacht A et al. Identification and characterization of RNA guanine-quadruplex binding proteins. Nucleic Acids Res. Jun;42(10):6630-44 (2014).
24. Haeusler et al. C9orf72 nucleotide repeat structures initiate molecular cascades of disease. Nature 507, 195©C200 (2014).
25. McRae EKS et al. Human DDX21 binds and unwinds RNA guanine quadruplexes. Nucleic Acids Res. Jun 20;45(11):6656-6668 (2017).
26. Serikawa T et al. Comprehensive identification of proteins binding to RNA G-quadruplex motifs in the 5' UTR of tumor-associated mRNAs. Biochimie. Jan;144:169-184 (2018).
27. Herdy B et al. Analysis of NRAS RNA G-quadruplex binding proteins reveals DDX3X as a novel interactor of cellular G-quadruplex containing transcripts. Nucleic Acids Res. Nov 30;46(21):11592-11604 (2018).
28. Yu H et al. G4Atlas: a comprehensive transcriptome-wide G-quadruplex database. Nucleic Acids Res. Jan 6;51(D1):D126-D134 (2023).
29. Bourdon S et al. QUADRatlas: the RNA G-quadruplex and RG4-binding proteins database. Nucleic Acids Res. Jan 6;51(D1):D240-D247 (2023).
30. Qian SH et al. EndoQuad: a comprehensive genome-wide experimentally validated endogenous G-quadruplex database. Nucleic Acids Res. Jan 5;52(D1):D72-D80 (2024).
31. Zhong HS et al. G4Bank: A database of experimentally identified DNA G-quadruplex sequences. Interdiscip Sci. Sep;15(3):515-523 (2023).
32. Birney E et al: An overview of Ensembl. Genome Res. May;14(5):925-8 (2004).
╣┘ŠWŻ║www.aksomics.com
ļŖįÆŻ║800-820-5058 400-886-5058 021-64451989
ĄžųĘŻ║╔Ž║Ż╩ąķhąąģ^ĻÉąą╣½┬Ę2168╠¢ŲųĮŁųŪ╗█ÅVł÷10C┤▒4śŪ
Į±╚šäėæB | ╚╦▓┼╩ął÷ | ą┬╝╝ągīŻÖ┌ | ųąć°┐ŲīW╚╦ | įŲš╣┼_ | BioHot | įŲųv╠├ų▒▓ź | Ģ■š╣ųąą─ | ╠žārīŻÖ┌ | ╝╝ąg┐ņėŹ | ├Ō┘Mįćė├
░µÖÓ╦∙ėą ╔·╬’═©
Copyright© eBiotrade.com, All Rights Reserved
┬ōŽĄą┼ŽõŻ║
╗øICPéõ09063491╠¢